
Energía térmica
Las moléculas que conforman la materia vibran y por lo tanto poseen energía cinética. Esta energía se llama energía térmica y forma parte de la denominada energía interna. Todos los elementos materiales que se encuentren a una temperatura superior al cero absoluto poseen energía térmica. Al igual que otras formas de energía, en el Sistema Internacional, se mide en joules (J).Una forma de entender el concepto de energía térmica de un cuerpo puede ser como la suma de la energía cinética de todas sus moléculas.
La energía térmica total que posee un cuerpo no solo depende de su temperatura sino también de su masa y su capacidad calorífica. En las próximas secciones se explican más detalladamente estos conceptos.
Temperatura
Como mencionamos, las moléculas que conforman la materia vibran y por lo tanto tienen energía cinética. La temperatura es una medida promedio de la energía cinética de un conjunto de partículas. Se mide con un termómetro.En el Sistema Internacional la temperatura se mide en grados kelvin (°K). Sin embargo es usual encontrarla en otras unidades tales como el grado centígrado (también llamado grado celsius y representado por el símbolo °C) o el grado fahrenheit (°F).
La temperatura está directamente relacionada con la energía térmica de un cuerpo aunque no es una medida de ello. Por ejemplo, un cuerpo de menor temperatura que otro podría tener mayor energía térmica si tiene mayor masa.
Conversión entre unidades de temperatura
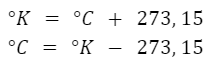
°K = Temperatura en grados kelvin [°K]
°C = Temperatura en grados centígrados [°C]
Calor
Se denomina calor a la energía térmica que se transfiere desde o hacia un sistema termodinámico. En un concepto muy similar al de energía térmica aunque hace referencia a energía térmica transferida. Debido a que se trata de una forma de energía, en el Sistema Internacional se mide en joules (J).Existen otras unidades utilizadas para medir el calor como por ejemplo la caloría. Se define a una caloría (cal) como la cantidad de energía que se le debe proporcionar a un gramo de agua para aumentar su temperatura un grado. Una caloría es equivalente a 4,184 J. Esta unidad también suele denominarse caloría-gramo para diferenciarla de la kilocaloría, explicada a continuación.
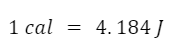
La kilocaloría es un múltiplo de la caloría que equivale a 1000 calorías, es decir a 4184 joules. Es la cantidad de energía térmica necesaria que debe suministrarse a un kilogramo de agua para aumentar su temperatura en un grado centígrado. Suele llamarse también Caloría (con la c en mayúscula) o caloría-kilogramo. Su abreviatura es “kcal” o más usualmente “Cal” (también con la c en mayúscula para diferenciarla de la caloría).
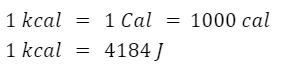
Relación entre calor y temperatura
- El calor hace referencia a la cantidad total de energía térmica que se transfiere a un cuerpo y se mide en unidades de energía tales como el joule o la caloría.
- La temperatura hace referencia a la energía cinética promedio de un conjunto de partículas debido a su vibración. Se mide en unidades tales como el grado kelvin, el grado centígrado o el grado fahrenheit.
- Si se aporta calor a un cuerpo entonces aumenta su temperatura.
- Un cuerpo a mayor temperatura que otro no necesariamente tiene mayor energía térmica.
Volver a calor
Volver a home